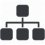A maior parte das imagens utilizadas neste site pertencem a terceiros, que gentilmente permitiram
sua utilização, assim sendo, não podemos autorizar a utilização das imagens deste site.
© COPYRIGHT 2000 - CIENCIA-CULTURA.COM - TODOS OS DIREITOS RESERVADOS - Responsável - Ricardo Pante
Como estudar física?
O que é ciência?


1.1 O que é a física? Como trabalham os físicos?



1.1.b A Física faz perguntas sobre o mundo natural
Na
época
dos
experimentos
de
Rutherford,
o
modelo
atômico
aceito
era
o
chamado
modelo
do
"pudim
de
ameixas"
,
proposto
por
J.
J.
Thomson.
Foi
Thomson
quem
descobriu
o
elétron,
e
ele
acreditava
que
o
átomo
era
uma
esfera
de
carga
positiva
onde
os
elétrons
estariam
distribuídos
aleatoriamente,
como
ameixas
espalhadas
na
massa
de
um
pudim
de
Natal.
Naquele
período,
a
existência
dos
prótons e nêutrons ainda era desconhecida.
No
início
do
século
XX,
Ernest
Rutherford
passou
a
investigar,
entre
outras
coisas,
a
estrutura
do
átomo
—
considerada
na
época
uma
partícula
fundamental
do
mundo
natural.
Embora
os
átomos
não
possam
ser
vistos
a
olho
nu,
eles
pertencem
ao
mundo
natural
e
podem ser estudados por meio das ferramentas da ciência.
1.1.c A Física tem como objetivo explicar o mundo natural
As
investigações
de
Rutherford
buscavam
entender
um
mistério
aparentemente
pequeno,
mas
profundamente
revelador
sobre
o
mundo natural: a estrutura do átomo.
Para
isso,
ele
utilizou
partículas
alfa
—
que
são
núcleos
de
hélio
(átomos
de
hélio
sem
seus
elétrons),
com
carga
positiva
.
Em
uma
série
de
experimentos,
Rutherford
observou
que,
ao
incidir
um
feixe
de
partículas
alfa
sobre
uma
f
iníssima
folha
de
ouro
,
a
maior
parte
das
partículas
atravessava
a
folha
sem
desvio
significativo.
No
entanto,
algumas
eram
levemente
desviadas,
e
outras,
em
menor
quantidade,
eram refletidas em ângulos muito grandes.
Rutherford queria entender o que esse comportamento das partículas alfa
revelava sobre a verdadeira estrutura interna do átomo.
1.1.d A Física trabalha com ideias testáveis
Antes
de
1910,
tanto
Rutherford
quanto
muitos
outros
físicos
acreditavam
que
a
carga
positiva
e
a
massa
do
átomo
estavam
distribuídas de forma homogênea por todo seu volume
, com os elétrons dispersos nesse meio.
Esse
modelo,
chamado
de
"pudim
de
ameixas"
,
imaginava
os
elétrons
(
as
"ameixas")
mergulhados
numa
massa
positiva
(o
"pudim").
Para testar essa ideia,
Rutherford disparou partículas alfa contra uma folha de ouro extremamente fina.
Se
o
modelo
estivesse
correto,
a
carga
positiva
e
a
massa
estariam
distribuídas
uniformemente,
e
as
partículas
alfa
deveriam
passar
quase
sem
desvios,
sofrendo
apenas
pequenas
deflexões
.
No
entanto,
os
desvios
observados
indicaram
que
a
massa
e
a
carga
positiva
estavam
concentradas
em
uma
região
muito
pequena
do
átomo
—
levando
à
formulação
de
um
novo
modelo
atômico,
com
um núcleo central denso.
1.1.e A Física depende de evidências
O
laboratório
de
Ernest
Rutherford
testou
o
modelo
atômico
vigente
à
época,
disparando
um
feixe
de
partículas
alfa
sobre
uma
fina
folha
de
ouro.
Segundo
o
modelo
de
Thomson
—
o
“pudim
de
ameixas”
—,
esperava-se
que
essas
partículas
atravessassem
a
folha
com
apenas
pequenos
desvios,
já
que,
de
acordo
com
esse
modelo,
a
carga
positiva
e
a
massa
do
átomo
estariam
distribuídas
uniformemente.
No
entanto,
a
evidência
observada
foi
surpreendente:
a
maior
parte
das
partículas
alfa
realmente
atravessou
a
folha
de
ouro
sem
grandes
alterações
em
sua
trajetória,
como
se
passassem
por
espaço
vazio.
No
entanto,
algumas
partículas
foram
desviadas
em
ângulos
acentuados
e,
mais
surpreendentemente,
outras
chegaram
a
ser
refletidas
de
volta
—
como
se
tivessem
colidido
com
uma
estrutura
extremamente
densa
e
sólida
dentro
do
átomo.
Se
os
átomos
de
ouro
fossem
de
fato
como
descrito
no
modelo
do
pudim
de
ameixas,
todas
as
partículas
alfa
deveriam
ter
passado
praticamente
sem
resistência.
O
fato
de
algumas
terem
sido
refletidas
para
trás
indicava
que
havia algo muito diferente na estrutura do átomo.
A
partir
dessas
evidências,
Rutherford
concluiu
que
o
modelo
de
Thomson
estava
incorreto.
O
átomo,
na
verdade,
seria
composto
majoritariamente
por
espaço
vazio,
e
sua
carga
positiva
estaria
concentrada
em
uma
pequena e densa região central: o núcleo.

1.1.g Ideias científicas levam a pesquisas contínuas
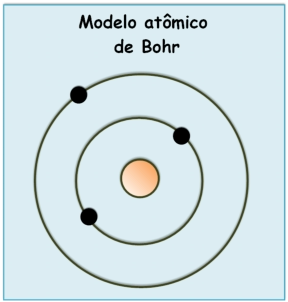
Niels
Bohr
baseou-se
no
trabalho
de
Ernest
Rutherford
para
desenvolver
o
modelo
do
átomo
mais
comumente
retratado
em
livros
didáticos:
um
núcleo
orbitado
por
elétrons
em
diferentes
níveis.
Apesar
das
novas
questões
que
levantou
(por
exemplo,
por
que
elétrons
em
órbita
com
carga
negativa
não
entram
em
espiral
até
o
núcleo
com
carga
positiva?),
esse
modelo
foi
poderoso
e,
com
mais
modificações,
levou
a
uma
ampla
gama
de
previsões
precisas
e
novas
descobertas,
incluindo
a
previsão
do
resultado
de
reações
químicas, a determinação da composição de estrelas distantes e a concepção da bomba atômica.
Concluindo
Ernest Rutherford e seus colegas agiram de maneira tão notável que fizeram a ciência avançar:
•
Eles
compreenderam
o
conhecimento
relevante
em
sua
área.
Rutherford
estudava
Física
há
mais
de
20
anos
quando
propôs
a ideia do núcleo.
•
Eles
expuseram
suas
ideias
a
testes.
Mesmo
que
sua
visão
original
do
átomo
sugerisse
que
nenhum
retroespalhamento
deveria
ocorrer,
Rutherford
decidiu
procurar
partículas
alfa
retroespalhadas
de
qualquer
maneira,
apenas
para
ser
minucioso.
•
Eles
assimilaram
as
evidências.
Quando
seus
resultados
experimentais
não
apoiaram
o
modelo
"pudim
de
ameixas
do
átomo,
em
vez
de
escrever
esses
resultados
como
uma
anomalia,
eles
modificaram
suas
ideias
originais
à
luz
das
novas
evidências.
•
Eles
comunicaram
abertamente
suas
ideias
para
que
outros
físicos
também
pudessem
testá-las.
Rutherford
publicou,
em
1911, em uma revista científica, os resultados experimentais, uma descrição de seu raciocínio e a ideia do núcleo.
•
Agiram
com
integridade
científica.
Em
seu
artigo
sobre
o
tema,
Rutherford
atribuiu
crédito
de
forma
justa
(citando
as
contribuições
de
seus
colegas,
Geiger
e
Marsden)
e
relatou
seus
resultados
honestamente
–
mesmo
quando
os
resultados
experimentais e seus cálculos teóricos não correspondiam perfeitamente.
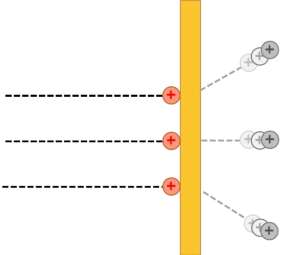
Átomos
de
lítio
esquematizados
nos
modelos
de
Rutherford
e
de
Bohr.
O
modelo
de
Rutherford
não
faz
distinção
alguma
entre
os
elétrons,
enquanto
o
de
Bohr
posiciona-os
orbitais com níveis de energia bem definidos.

“O
que
é
física?
Uma
maneira
de
responder
a
esta
questão
é
descrever
a
física
como
o
estudo
do
movimento,
energia,
calor,
ondas,
som,
luz,
eletricidade,
magnetismo,
matéria,
átomos,
moléculas
e
núcleos.
Esta
descrição,
além
de
soar
como
o
índice
de
um
livro
de
física
do
ensino
médio,
não
especifica
realmente
a
natureza
da
física.
A
física
não
é
apenas
o
estudo
dos
fenómenos
naturais
listados
acima,
mas
é
também
um
processo;
um
processo
que
tem
dois
aspectos
distinguíveis.
A
primeira
delas
é
simplesmente
a
aquisição
de
conhecimento
do
nosso
ambiente
físico.
A
segunda,
e
talvez
mais
interessante,
é
a
criação
de
uma
visão
de
mundo,
que
fornece
uma
estrutura
para
a
compreensão
do
significado
desta
informação.
Estas
duas
atividades
não
são
de
forma
alguma,
independentes
uma
da
outra.
É
necessária
uma
visão
de
mundo
para
adquirir
novos
conhecimentos
e
vice-versa, é necessário conhecimento para criar uma visão de mundo.”
The Poetry of Physics and the Physics of Poetry
Robert K Logan (University of Toronto, Canada)
Créditos:
(1)
https://undsci.berkeley.edu/understanding-science-101/what-is-science/a-science-checklist/
(2)
Entendendo a Ciência 101 - Entendendo a Ciência (berkeley.edu); acesso em 16 nov. 2023.
(3) https://undsci.berkeley.edu/understanding-science-101/; acesso em 16 nov. 2023.
https://en.wikipedia.org/wiki/Ernest_Rutherford
https://en.wikipedia.org/wiki/Rutherford_scattering_experiments
Os
cientistas
envolvidos
nessa
investigação
cumpriram
as
cinco
etapas
de
conduta
do
cientista.
Dessa
forma
–
e
a
julgar
pelos
outros
itens
da
lista
–,
essa
investigação
da
estrutura
atômica
está
intensamente
dentro da alçada da ciência.
Contudo,
o
papel
desempenhado
pela
física
é
vasto.
O
guia
da
ciência
ou,
em
especial,
da
física
integra-se
com
um
vasto
conjunto
de
esforços
humanos.
Quando
pretendemos
estudar
a
queda
de
um
corpo,
a
nossa
pretensão
é
chegar
a
um
resultado
preciso,
possivelmente
uma
lei
que
descreva
como
o
fenômeno
ocorre,
o
que
nos
permitiria
calcular,
por
exemplo,
o
tempo
de
queda do corpo até atingir o chão.
É bom lembrar que a física tem seus
Índice das aulas de física
Quando
partículas
alfa
carregadas
positivamente
são
atiradas
contra
uma
fina
folha
de
ouro,
elas
mudam
de
direção.
Se
a
massa
positiva
de
um
átomo
e
seus
elétrons
fossem
distribuidos
uniformemente…...
então
o
esperado
era
que
as
minúsculas
partículas
alfa
ao
passarem
através
da
fina
folha
de
ouro,
sofressem
um pequeno desvio.
O
que
foi
observado
é
que
algumas
partículas
alfa
(positivas)
foram
repelidas
da
folha
de
ouro
em
quase
180
graus,
o
que
indica
que
os
átomos
têm
a
sua
carga
positiva concentrada em uma massa densa
Sir Joseph John Thomson 1856 - 1940
Foi
um
físico
britânico,
a
quem
se
atribui
a
descoberta
do
elétron,
a
primeira
partícula
subatômica
a
ser
encontrada.
Fonte - Wikipédia - domínio público
Ernest Rutherford (1871-1937)
Fonte:
Wikipedia.
Coleção
George
Grantham
Bain (Biblioteca do Congresso)
O
modelo
do
átomo
proposto
por
JJ
Thomson.
Inicialmente
pensava-se
que
os
átomos
continham
muitas
centenas
ou
milhares
de
elétrons.
Fonte - Wikipédia - domínio público
Autor - Tjlafave
Ernest Rutherford (à direita) e Hans Geiger no laboratório de física da Universidade de Manchester, Inglaterra, por volta de 1912.
Fonte:
a
permissão
da
Biblioteca
Alexander
Turnbull,
Wellington,
Nova
Zelândia,
deve
ser
obtida
antes
de
qualquer
reutilização
desta
imagem. Número de referência: PAColl-0091-1-011.
Se
você
entendeu
como
atua
um
cientista,
você
não
terá
nenhuma
dificuldade
como
é
na
física.
A
física
faz
parte
do
grupo
que
chamamos ciências da natureza, cujo objetivo é estudar a natureza em seus aspectos mais gerais e fundamentais.
A
física
se
preocupa
com
a
matéria,
envolve
o
estudo
da
matéria,
seus
constituintes
fundamentais,
seu
movimento
e
comportamento
no
espaço
e
tempo,
e
as
entidades
relacionadas
à
energia
e
à
força.
A
física
é
uma
das
disciplinas
científicas
mais
fundamentais, tendo como objetivo principal compreender como o universo se comporta.
Por
ser
uma
área
básica
na
ciência,
a
física
utiliza
o
método
científico
para
formular
e
testar
hipóteses
e
utiliza
os
resultados
dos
experimentos
para
formular
leis,
expressas,
geralmente,
na
linguagem
da
matemática
e
que
podem
então
ser
usadas
para
prever
outros fenômenos.
Um
bom
exemplo
de
como
atuam
os
físicos
é
analisar
as
etapas
da
investigação
realizada
por
Ernest
Rutherford
sobre
a
estrutura
do
átomo.
Para
essa
análise,
seguiremos
a
lista
das
principais
características
da
ciência,
apresentada
anteriormente.
Ao
adaptar a lista para a física, têm-se que:
•
A física faz perguntas sobre o mundo natural.
•
Tem como objetivo explicar o mundo natural.
•
A física trabalha com ideias testáveis.
•
A física depende de evidências.
•
A física está inserida na comunidade científica.
•
Ideias científicas levam a pesquisas contínuas.
Ernest
Rutherford
foi
um
pesquisador
pioneiro
em
física
atômica
e
nuclear
e
é
descrito
como
"o
pai
da
física
nuclear"
e
um
dos
maiores
experimentalistas
"desde
Michael
Faraday".
Em
1911,
ele
defendeu
que
os
átomos
têm
sua
carga
positiva
concentrada
em
um pequeno núcleo, e, desse modo, criou o modelo atômico de Rutherford, ou modelo planetário do átomo.
(1)
1.1.a Introdução
limites:
algumas
questões
que
são
uma
parte
importante
da
experiência
humana
não
podem
ser
respondidas
no
contexto
da
física
(ou
da
ciência).
Por
isso,
a
Física
não
é
tudo,
mas
é
importante.
Ela
ajuda-nos
a
construir
um
conhecimento
acerca
do
mundo
natural
– conhecimento que pode ser aproveitado para melhorar as nossas vidas e resolver problemas.
Bases
da
Física


Assim,
quando
as
partículas
alfa,
também
carregadas
positivamente,
atravessavam
o
átomo,
a
maioria
passava
livremente,
mas
algumas
colidiam
com
o
núcleo
e
eram
fortemente
repelidas,
como
acontece
quando
se
tenta
aproximar
os
polos
positivos
de
dois
ímãs.
A
nova
ideia
de
que
os
átomos
possuem
um
núcleo
positivo
denso
era
testável
e,
por
isso,
pôde
ser
confirmada
por
meio
de
diversos
experimentos
independentes
realizados
por
outros
pesquisadores,
reforçando
a
confiabilidade
dessa
nova
concepção
atômica.
1.1.f A física está inserida na comunidade científica
Embora
Ernest
Rutherford
tenha
tido
a
ideia
de
que
os
átomos
têm
núcleos
carregados
positivamente,
a
pesquisa
que
levou
a
essa
ideia
foi
um
esforço
colaborativo:
Rutherford
foi
assistido
por
Hans
Geiger,
e
o
experimento
crítico
de
espalhamento
alfa
foi
realmente realizado por Ernest Marsden, um estudante de graduação que trabalhava no laboratório de Rutherford.
Além
disso,
após
a
descoberta
da
disposição
do
átomo,
Rutherford
publicou
uma
descrição
da
ideia
e
das
evidências
relevantes, divulgando-as à comunidade científica para exame rigoroso e avaliação. E eles examinaram minuciosamente.
Niels Bohr notou um problema com o modelo do átomo de Rutherford: não havia nada que impedisse os elétrons em órbita
executar uma trajetória em espiral em direção ao núcleo do átomo, causando o colapso de tudo! Bohr modificou o modelo básico de
Rutherford propondo que os elétrons estabeleceram níveis de energia, o que ajudou a resolver o problema e rendeu a Bohr o Prêmio
Nobel. Desde então, muitos outros cientistas desenvolveram e modificaram o modelo de Bohr.
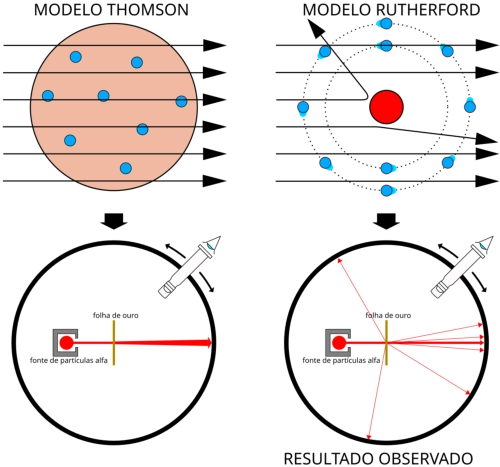
Os resultados do experimento Geiger- Marsden
A
figura
é
uma
comparação
entre
os
resultados
esperados
para
o
experimento
de
Geiger–Marsden
de
acordo
com
o
modelo
de
Thomson
(figura
à
esquerda).
Se
o
modelo
de
Thomson
estivesse
correto,
todas
as
partículas alfa deveriam ter passado pela folha com dispersão mínima.
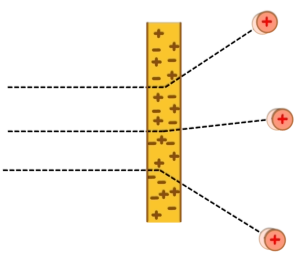
No
modelo
de
Rutherford
(figura
à
direita),
o
que
Geiger
e
Marsden
observaram
foi
que
uma
pequena
fração
de
partículas
alfa
sofreram
uma
forte deflexão.
- Autor: By Kurzon - Wikipedia
fonte de partícu-
…las alfa.
fonte de partí-..
culas alfa.
folha de ouro

folha de ouro
RESULTADO ESPERADO